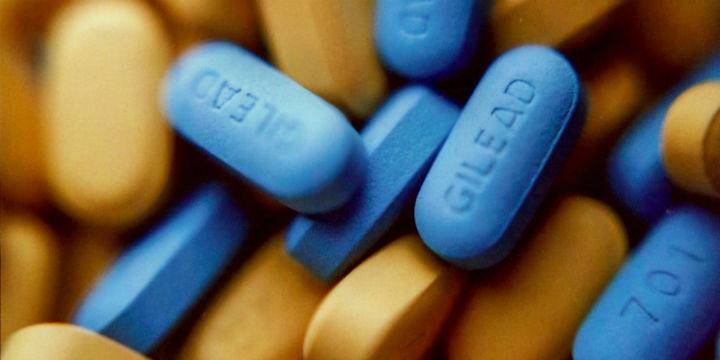
Auch in Europa könnte das HIV-Medikament Truvada schon bald zur Vorbeugung einer Infektion mit dem Virus zugelassen werden: Die Herstellerfirma Gilead hat bei der Europäischen Arzneimittelbehörde (EMA) einen Antrag auf eine Zulassungsänderung gestellt. Damit dürfte das Medikament auch zur Vorbeugung einer Ansteckung, die in diesem Fall Präexpositionsprophylaxe (PrEP) heißt, zugelassen werden. Seit 2005 ist Truvada in Kombination mit anderen antiretroviralen Wirkstoffen in Europa für die Behandlung von HIV-Infektionen zugelassen. Es ist derzeit das am häufigsten verschriebene antiretrovirale Arzneimittel in Europa.
Truvada in mehreren Ländern zur Vorsorge zugelassen
In Kombination mit Safer Sex reduziert eine tägliche Einahme von Truvada, einer Kombination der Wirkstoffe Tenofovir und Emtricitabin, das Risiko einer HIV-Infektion praktisch auf Null. In den USA ist Truvada deshalb seit 2012, in Kenia und Südafrika seit 2015 zur Vorbeugung zugelassen. Die US-Gesundheitsbehörde CDC hat im November 2015 sogar empfohlen, dass Menschen mit einem hohen Risiko Truvada zur PrEP einnehmen sollen. Dazu zählen der Behörde zufolge rund ein Viertel der schwulen und bisexuellen Männer, die sexuell aktiv sind.
In Australien, Brasilien, Kanada, Peru und Thailand sind entsprechende Anträge bereits gestellt wurden. Nun wurde ein solcher Antrag auch in Europa gestellt. Die EMA ist für die Zulassung von Medikamenten in allen Staaten der EU sowie in Norwegen, Island und Liechtenstein zuständig. Frankreich hat bereits vor Kurzem eine „temporäre Gebrauchsempfehlung“ für Truvada gegeben, um HIV-Infektionen zu verhindern.
Hohe Kosten als Argument gegen Verschreibung?
Problematisch sind allerdings Dosierung und Kosten von Truvada zur Vorbeugung einer Infektion mit HIV: So muss derzeit jeden Tag eine Tablette genommen werden, um einen Schutz zu erreichen. Damit müssen HIV-Negative die gleiche Dosis des Medikaments einnehmen, die auch HIV-Positive brauchen – mit den gleichen Nebenwirkungen wie Kopfschmerzen, Durchfall, Gewichtsabnahme oder Magenbeschwerden.
Klinische Untersuchungen prüfen jetzt, ob die Dosis für einen vorbeugenden Schutz vor dem Virus auch geringer sein kann. Erste Ergebnisse lassen darauf schließen, dass der Schutz auch aktiv sein könnte, wenn man Truvada nur jeden zweiten Tag nimmt.
Kein Ersatz für Kondome
Ein Ersatz für Kondome kann Truvada aber nicht sein: Die PrEP stelle lediglich „eine zusätzliche Schutzmöglichkeit für einige Gruppen dar“, betont die Deutsche Aids-Hilfe (DAH) in einer Stellungnahme zum Antrag von Gilead. Dazu gehörte „vor allem für eine kleine Gruppe von schwulen Männern in Frage, die ein sehr hohes HIV-Risiko haben, zum Beispiel, weil es ihnen aufgrund ihrer Lebensumstände schwerfällt, sich mit Kondomen zu schützen“.
Derzeit kostet eine Monatsdosis Truvada, bestehend aus 30 Tabletten, in Deutschland oder Österreich mehr als 800 Euro. In den USA bezahlen private Krankenkassen die Medikamente auch zur Vorbeugung einer Ansteckung. Ob das auch die österreichische Sozialversicherung tun würde, ist unklar.
US-Krankenversicherungen unterstützen PrEP
Durch die Unterstützung der Krankenkassen ist in den USA die Zahl jener, die Truvada für die PrEP nehmen, stark angestiegen. So sollen einer aktuellen Studie aus dem Bundesstaat Washington zufolge 31 Prozent der „besonders gefährdeten Männer, die Sex mit Männern haben“, bereits mindestens einmal PrEP eingenommen haben. 2012 habe der Anteil noch bei fünf Prozent gelegen.
Neben der Verhinderung einer HIV-Infektion vor einem Risikokontakt kann Truvada auch eine Infektion mit dem Virus verhindern, nachdem der Kontakt erfolgt ist: Das Medikament wird in Europa bereits zusammen mit einem anderen Medikament auch für die Post-Expositionsprophylaxe (PEP) verwendet. Dafür müssen die Arzneimittel innerhalb von 24 Stunden nach dem Risikokontakt eingenommen werden.